有限蛋白水解质谱技术(Limited Proteolysis Mass Spectrometry,LiP-MS)是研究小分子化合物(天然产物、代谢物等)与蛋白质相互作用,揭示蛋白结构动态变化的高通量质谱筛选技术。本公司推出LiP-MS药物靶点筛选解决方案,包含三种研究目的场景
01
技术原理
有限水解(LiP)的概念是指在生理状态下蛋白酶对蛋白的不完全酶切。研究表明,生理状态下折叠的蛋白具有较强的抗酶切能力,所以实验中想要实现对蛋白的完全酶切需要先对蛋白进行变性处理(去折叠)(图1)。而在生理状态下,折叠蛋白的不完全酶切也需要蛋白酶识别位点的暴露,通常涉及到多达12以上氨基酸残基肽段的构象变化(局部展开),这依赖于蛋白的动态变化,蛋白表面肽段的柔性变化可能会形成这种能被蛋白酶识别切割的位点。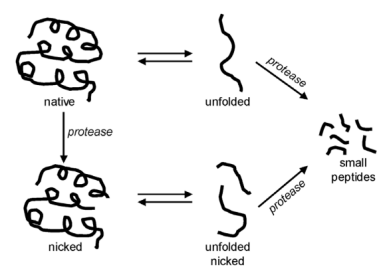
图1:蛋白有限水解示意图
LiP-MS利用有限水解的原理来识别小分子药物作用的蛋白靶点。具体来讲,生理状态下蛋白的动态变化会暴露出表面肽段的酶切位点,但是小分子药物与靶蛋白结合后,会在整体或者局部水平稳定蛋白的结构,这使得蛋白表面的肽段暴露和被蛋白酶酶切的可能性大大降低(图2)。
在这个理论背景下,设置药物处理组与溶剂处理的对照组,同时以非特异性的蛋白酶进行处理,会在药物结合的靶蛋白上形成酶切位点(肽段)的差异,最后通过质谱检测来定量筛选出组间差异的肽段(蛋白),最终可以确认为药物作用的结合靶点(图3)。
图2:小分子配体(药物)稳定蛋白结
图3:LiP-MS流程图
02
产品优势
简单便捷
真实直接
数据驱动
直接结论
验证数据
03
产品介绍
LiP-MS药物靶点筛选
药物靶点研究最常见的场景是有了一个有效的药物,但是不清楚这个药物作用的具体靶点和机制。这个时候可以进行蛋白质组水平的LiP-MS药物靶点筛选。客户提供原始的细胞或组织及药物,谱度众合实验室在非变性条件下提取疾病模型细胞/组织中的全部蛋白,分别使用药物和溶剂进行处理,随后进行有限水解实验,通过质谱高通量筛选两组间差异肽段,实现在整体蛋白水平筛选药物作用的蛋白靶点。
送样要求
1. 至少6个给药前样本(药物处理组3个,溶剂对照组3个;如需增加不同浓度或者不同药物处理组,每组增加3个样本);
2. 单个样本起始细胞量建议>1*10E7(组织样本>5mg);药物用量:摩尔分子质量/10(μg),例如分子量1000的药物,需要100μg的量;或者20μL*5mM的药物溶液。
收集细胞/组织样本时需以PBS清洗干净,样本不含有任何去垢剂/变性剂成分。
LiP-MS药物-蛋白结合域分析
该产品应用于一个特殊的药物靶点研究场景:已经明确了药物作用的靶蛋白,但是不清楚药物作用在蛋白上的哪个位置(区域),可以通过对重组蛋白的LiP-MS实验来实现研究目的。客户提供纯化重组蛋白及药物,谱度众合实验室进行体外的重组蛋白和药物分子结合实验,随后进行有限水解实验,通过高分辨质谱来分析药物作用所产生的差异肽段,结合分子对接可以获得明确的药物-蛋白结合区域信息。
送样要求
1.至少6个给药前样本(药物处理组3个,溶剂对照组3个;如需增加不同浓度或者不同药物处理组,每组增加3个样本);
2.单个样本起始重组蛋白量建议>5μg(总量大于30μg,浓度不低于0.05μg/μL);
3.重组蛋白溶液中不含有任何去垢剂/变性剂成分。
LiP-MS药物机制研究
该产品用于体内/活细胞给药条件下筛选药物靶点,同时提供药物进入机体/细胞后引起的生理/病理变化(蛋白表达变化),以提供药物作用分子机制。客户提供经药物/溶剂对照处理后的细胞/组织样本,谱度众合实验室分成胰蛋白酶直接处理的定量比较组和有限水解处理后的结构比较组。通过定量比较组可以得到药物处理下蛋白表达变化结果。结构比较组数据经过定量比较组校正之后得到药物作用后蛋白结构变化信息(肽段差异),进而筛选药物作用靶点蛋白。

图4:LiP-MS药物机制研究实验方案
送样要求
1.至少12个给药/溶剂处理后的样本(药物处理组3个,溶剂对照组3个;药物处理有限水解组3个,溶剂对照组有限水解组3个);
2.单个样本起始细胞量建议>1*10E7(组织样本>5mg);
3.收集细胞/组织样本时需以PBS清洗干净,样本不含有任何去垢剂/变性剂成分。
04
报告结果
我们将LiP-MS的实验结果分成四个板块进行展示。其中第一部分是质谱检测结果的质控;第二部分差异分析及候选靶点筛选结果是主要的靶蛋白筛选结果,也是文章里使用的主要结果;第三部分生信功能分析与潜在靶点挖掘提供对第二部分筛选出的候选靶点的生信功能富集分析,可以辅助我们挑选最终的靶蛋白。第四部分靶蛋白结构分析与分子对接提供靶蛋白与药物分子的结合信息,可以作为辅助验证的结果。
[1].蛋白质组学检测及质控结果
图5:蛋白质组学检测质控数据
质谱质控结果,包括肽段长度分布、肽段电荷分布、蛋白肽段数目分布,肽段酶切类型分布
符合理论预期的质控结果能证明项目在实验处理和质谱检测阶段的稳定性。例如,项目使用蛋白酶K处理,肽段酶切类型中半特异性酶切肽段占比较高。
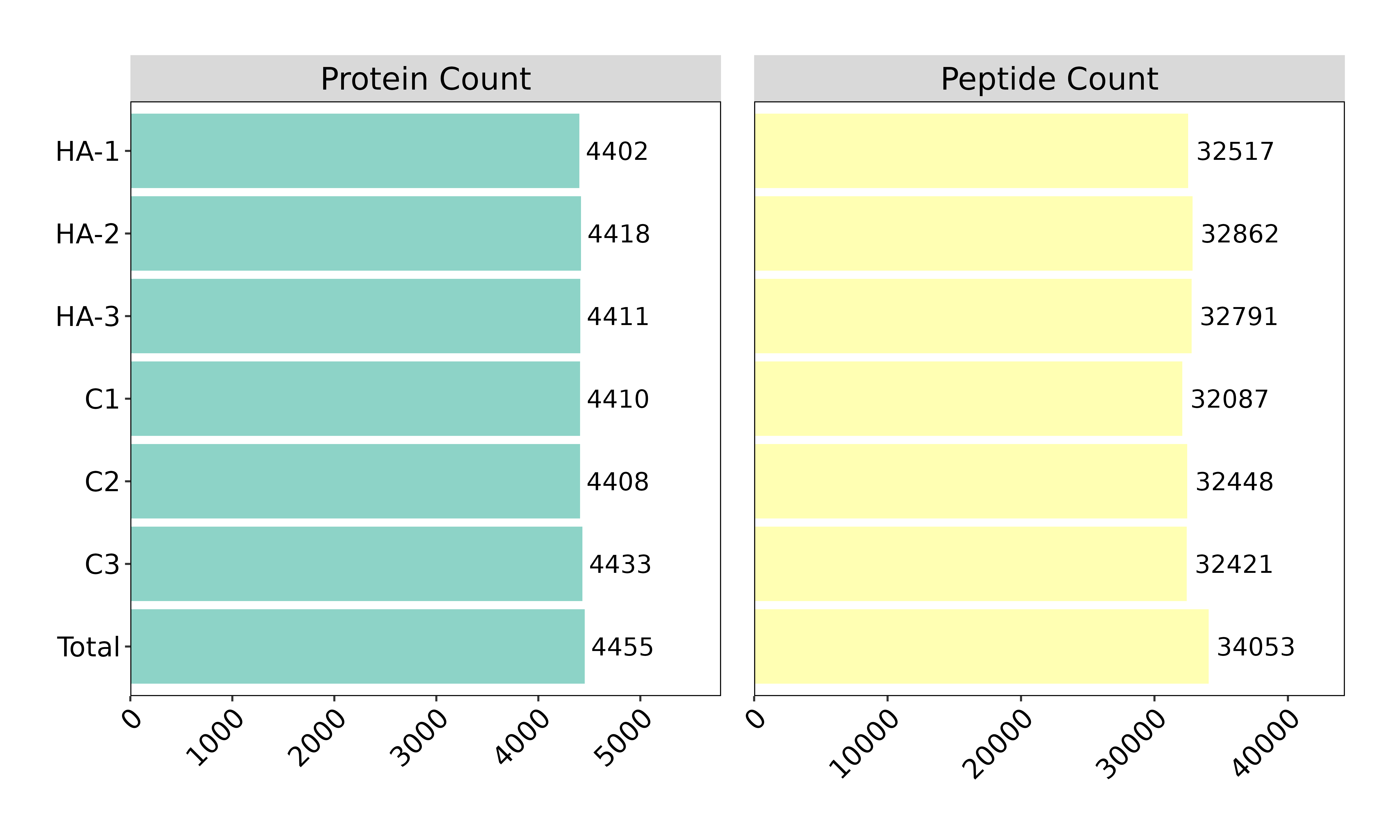
图6:项目蛋白肽段鉴定数据
实验样品通过布鲁克高性能Tims-tof pro质谱仪进行4D-DIA检测分析。项目在六个样品中共定量到了34053条unique肽段,归属于4455个unique蛋白。其中各组重复实验样品的蛋白肽段鉴定数据如图。
[2].差异分析及候选靶点筛选结果
图7:肽段定量差异分析火山图与热图
对比较组的肽段定量数据进行差异倍数计算和T检验,筛选出药物处理组样品中的差异变化肽段。差异肽段所对应的蛋白即为药物潜在靶蛋白,是项目中筛选药物靶点的核心部分结果。
[3].生信功能分析与潜在靶点挖掘

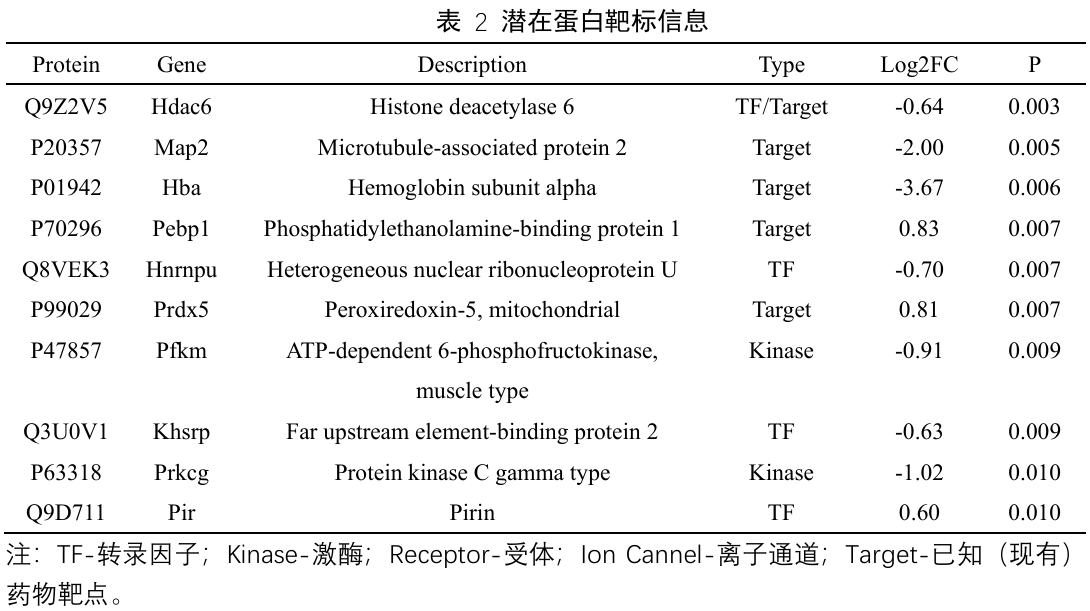
图8:生信功能分析与潜在靶点挖掘
注释富集分析,项目中包括GO、KEGG富集分析,蛋白互作网络(PPI)分析。潜在靶点挖掘(从AnimalTFDB4/PhosphoSitePlus/TCDB/TTD/CellChatDB等数据库中对实验所鉴定到的差异蛋白中的转录因子、激酶、离子通道蛋白、药物靶点和受体蛋白等潜在药物靶点蛋白进行注释)。这些分析内容可以为进一步的靶点筛选与验证提供理论支持。
[4].靶蛋白结构分析与分子对接
图9:蛋白结构标注与分子对接
LiP-MS技术通过对蛋白肽段的差异分析来筛选药物作用靶点,差异肽段在蛋白结构上的位置可以在一定程度上提供药物结合位置信息。在蛋白二级序列对本次实验所鉴定到的差异蛋白及肽段进行标注,分子对接通过计算机模拟计算药物和蛋白的结合力及结合位点,结合实验筛选到的蛋白差异肽段位置信息,能为药物和蛋白的相互作用提供有力的证据。
00
服务配置表
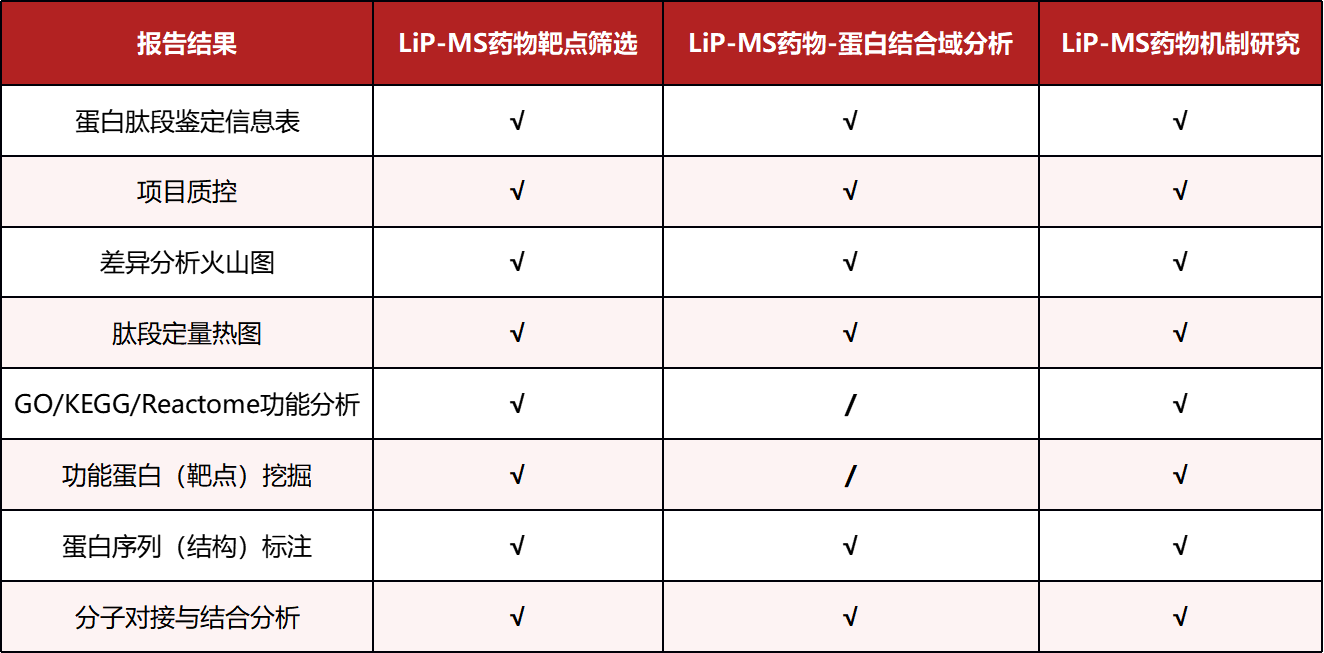
谱度众合是一家由武汉大学博士团队创办的科研服务企业,我们专注于利用质谱技术服务于生物标志物、药物靶点筛选、基础研究等蛋白质研究领域,我们在本专业细分领域持续深耕十几年,针对具体研究场景开发多种面向具体研究目的和论文发表需求的服务产品,助力于客户更轻松更高效的完成科研目标。
撰稿人:程锐锋
审核人:刘宜子


















